2026年4月15日,我院刘妍教授团队在《美国国家科学院院刊》(Proceedings of the National Academy of Sciences of the United States of America,PNAS)(中科院一区,IF=9.1) 杂志在线发表题为《FABP7 controls radial glial scaffold stability during human cortical development》的研究。该研究围绕脂肪酸结合蛋白7(FABP7)的功能展开,系统揭示了其在放射状胶质细胞(radial glia)支架稳定性及神经元迁移过程中的关键调控作用。

在大脑发育早期,放射状胶质细胞不仅可以作为神经干细胞产生神经元,还可以通过形成从脑室区到皮层表面的“支架结构”,引导新生神经元向正确位置迁移。这一结构的完整性对于皮层分层及功能形成至关重要。然而,尽管FABP7长期被视为放射状胶质细胞的经典标志物,其具体功能一直缺乏系统研究。
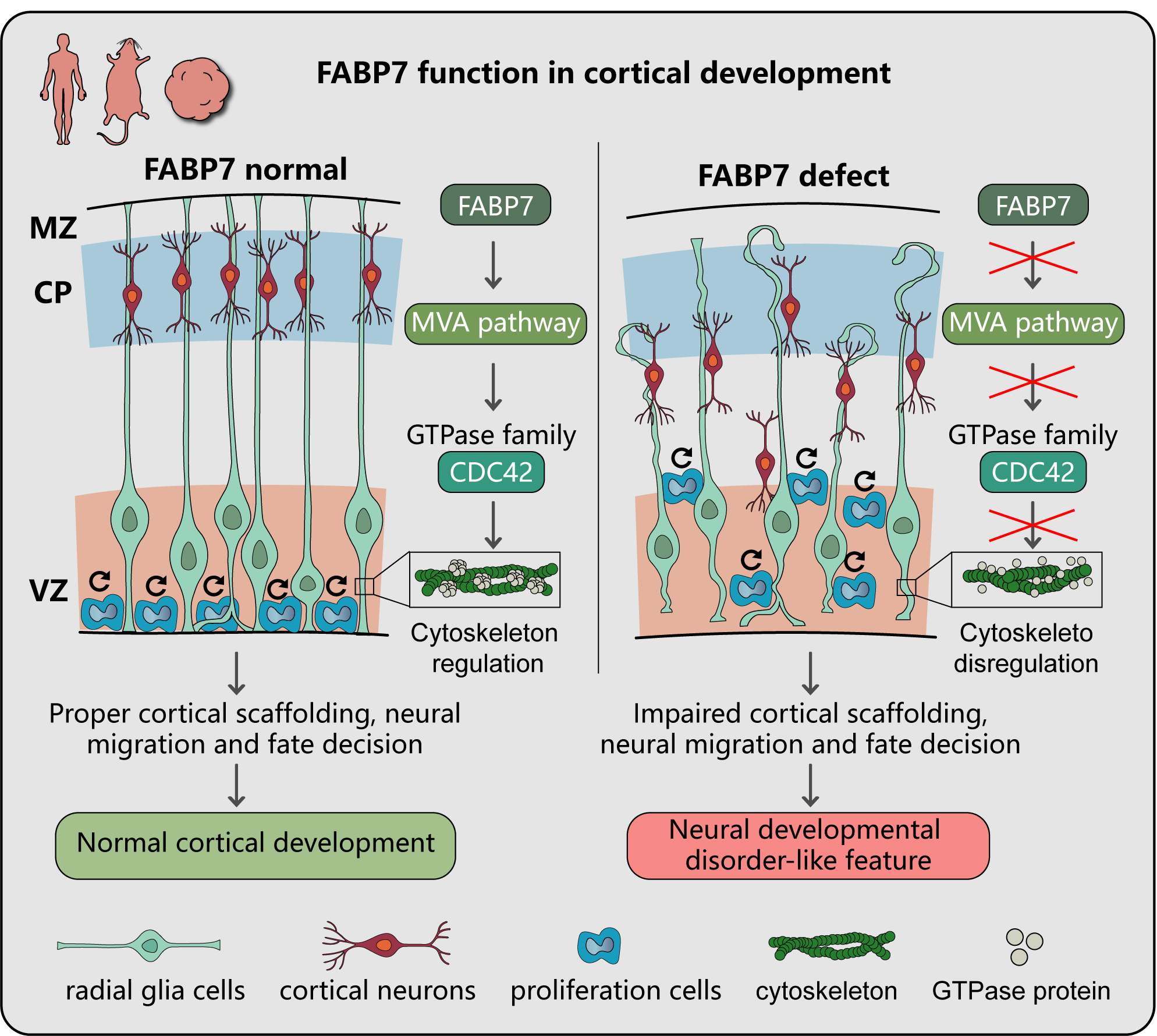
本研究整合了多种实验模型,包括人胎脑切片、小鼠胚胎脑组织、人源诱导多能干细胞来源的脑类器官以及类组装体模型,从多个层面深入解析FABP7的功能。研究发现,敲低FABP7会破坏放射状胶质细胞支架的结构,表现为纤维变短、排列紊乱,进而导致神经元迁移受阻及定位异常。在分子机制层面,单细胞转录组分析显示,FABP7缺失引发广泛的转录紊乱,尤其影响细胞骨架调控、小GTP酶相关信号及神经分化过程。进一步研究表明,FABP7通过调控甲羟戊酸(mevalonate, MVA)通路,影响小GTP酶CDC42的定位与活性,从而维持细胞骨架结构稳定。有意思的是,FABP7敲低后的转录特征与多种神经发育障碍,尤其是自闭症谱系障碍(ASD),呈现显著趋同;同时,在ASD患者来源的类器官中也观察到类似的胶质支架缺陷。
综上,该研究详细阐述了人大脑皮层发育早期FABP7调控放射状胶质支架发育的分子机制,并提出“FABP7–MVA–GTP酶–细胞骨架”这一调控轴,为理解人类大脑发育及相关疾病机制提供了重要理论基础。
本研究的通讯作者为我院刘妍教授、韩晓讲师,以及东南大学赵春杰教授、南京医科大学附属妇产医院程青主任。第一作者为我校博士生王源浩、张栩以及东南大学巴茹讲师。该研究得到国家自然科学基金青年A类(原杰青)项目、重点项目、面上项目,国家重点研发计划项目等项目的资助。
原文链接:https://doi.org/10.1073/pnas.2523130123
(撰稿/刘妍课题组;审核/陈宏山)


