1月20日,我院都述虎、李瑞、张爱霞团队在国际权威期刊Biomaterials(IF:14)上发表最新研究成果“Gint4.T-siHDGF chimera-capped mesoporous silica nanoparticles encapsulating temozolomide for synergistic glioblastoma therapy”。药学院费怀君博士、金阳老师和蒋南副教授为论文第一作者。
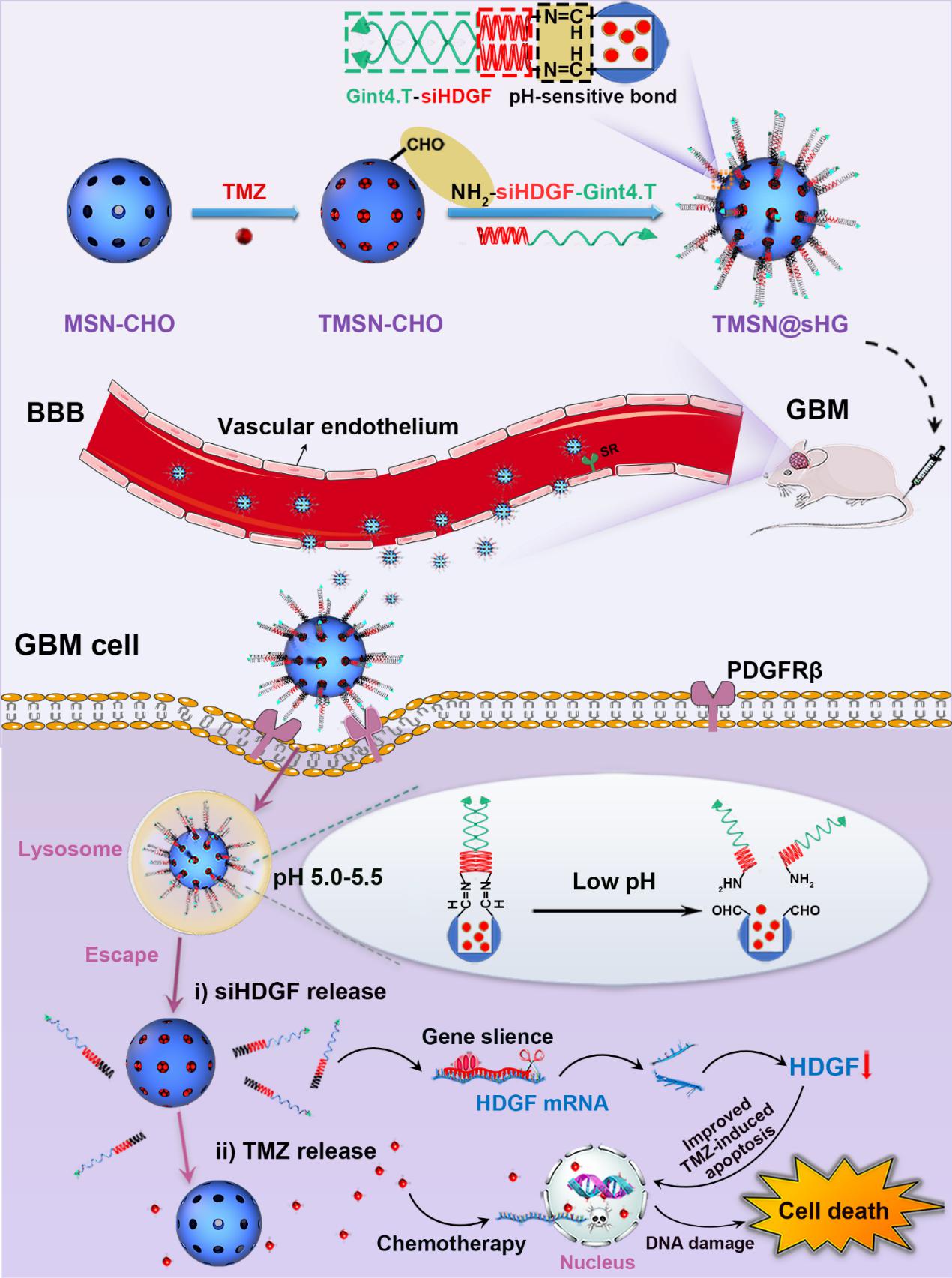
恶性脑胶质瘤 (GBM) 是中枢神经系统中侵袭性最强的肿瘤,具有预后差、复发率高和生存率低等特点。GBM患者的治疗金标准是手术切除,随后辅以放、化疗。但由于GBM组织的高度浸润性,手术并不能完全将其切除,临床治疗效果欠佳。替莫唑胺 (TMZ)作为美国FDA批准的烷化剂,是GBM最常用的一线治疗药物。但由于GBM细胞对TMZ的反应存在异质性,以及GBM细胞对TMZ固有的或获得性耐药,GBM依然是一种预后极差的疾病。随着科学技术的进步,各种纳米材料和技术被应用来开发以TMZ为基础的联合给药系统。然而,设计并制备同时实现高效的血脑屏障 BBB) 穿透、特异性靶向识别和序贯递送的共载药物材料仍然面临一个巨大的挑战。针对上述问题,本研究构建了一种基于嵌合体 (Gint4.T-siHDGF) 门控开关的介孔二氧化硅 (MSN) 负载化疗和基因药物 (TMZ和siHDGF) 共递送系统 (TMSN@sHG),用于时序递送基因和化疗药物到脑肿瘤部位。在该共递送系统中,首先将TMZ通过浸渍吸附,封装于MSN的孔道内,然后将具有“三合一”功能的嵌合体Gint4.T-siHDGF (siHDGF作为基因药物; Gint4.T则作为靶向基团; Gint4.T-siHDGF嵌合体作为门控开关) 通过苯甲酰亚胺键接枝于MSN的外表面。由于pH敏感的亚胺键在酸性条件下断裂,使得该共递送系统能够更早、更快地释放出siHDGF,随后TMZ缓慢且持续的释放到胶质母细胞瘤中。TMZ的延迟释放为提前下调HDGF蛋白致目标水平提供了充足的时间,从而增强了胶质母细胞瘤细胞对TMZ的敏感性。体内实验结果表明,该共递送系统具有良好的生物相容性、细胞摄取能力和高效的血脑屏障穿透能力,可显著抑制U87原位移植瘤的生长及明显延长小鼠的生存期。因此,该共递送系统将在治疗胶质母细胞瘤中,为时序控制释放siRNA和化疗药物提供了一个新方法。
本研究得到国家自然科学基金项目等资助。
原文链接:https://authors.elsevier.com/a/1iWLdWWN0%7EIAB
(撰稿/都述虎课题组;审核/陈宏山)
